RESUMO
OBJETIVO: Verificar a cicatrizaçao de queimaduras em áreas especiais através da aplicaçao da membrana bioativa de colágeno contendo ácido úsnico incorporado em lipossomas.
MÉTODO: Trata-se de um estudo de intervençao, descritivo e de campo, de comparaçao intraindividual, com abordagem quantitativa. A coleta de dados foi realizada na Unidade de Tratamento de Queimados (UTQ) do Hospital de Urgência de Sergipe (HUSE) durante três meses. A amostra foi composta por nove pacientes adultos, de ambos os sexos, apresentando duas áreas queimadas, selecionadas aleatoriamente em dois grupos: teste, no qual foram aplicadas as membranas bioativas; e controle, áreas submetidas à aplicaçao de óleo à base de ácido graxo essencial ou sulfadiazina de prata, padrao-ouro no tratamento de queimaduras. As imagens foram captadas por registro fotográfico padronizado e, em seguida, foi realizada a análise descritiva da queimadura, bem como o cálculo da área queimada, através do programa Image J®, antes e após intervençao.
RESULTADOS: Notou-se maior presença de tecido de granulaçao na área teste, bem como maior vascularizaçao, com cicatrizaçao mais homogênea e mais avançada, enquanto a área controle (C14) ainda se apresentava com mais exsudato e deposiçao de fibrina. Houve padrao de reduçao da área das queimaduras nos dois grupos analisados, com área mais reduzida no grupo teste (de 2,769 cm2 para 1,258 cm2) em relaçao ao controle (de 2,882 cm2 para 2,091 cm2).
CONCLUSAO: Observou-se melhora no aspecto clínico das lesoes, com cicatrizaçao mais acelerada e fisiológica nas áreas teste, em relaçao à área controle.
Palavras-chave:
Queimaduras. Cicatrização. Biotecnologia. Hospitalização. Pele.
ABSTRACT
OBJECTIVE: To verify the burns healing in special areas through the application of the bioactive membrane of collagen containing usnic acid incorporated into liposomes.
METHODS: This is an interventional, descriptive and field study, of individual comparison, with a quantitative approach. Data collection was performed at the Burn Treatment Unit of Sergipe Urgency Hospital during three months. The sample consisted of nine adult patients, of both sexes, presenting two burned areas, randomly selected in two groups: test, where the bioactive membranes were applied; and control, areas subject to the application of oil based on essential fatty acid or silver sulfadiazine, gold standard in burns treatment. The images were captured by the standardized photographic record and then the descriptive analysis of the burn was carried out, as well as the calculation of the burn area, through the Image J® program, before and after intervention.
RESULTS: There was a greater presence of granulation tissue in test area, as well as greater vascularization, with more homogeneous and more advanced healing, whereas the control area still presented with more exudate and fibrin deposition. There was reduction of burn area between groups, with lower area in test group (2.769 cm2 to 1.258 cm2) in relation to control group (from 2.882 cm2 to 2.091 cm2).
CONCLUSION: It was observed an improvement in the clinical aspect of the lesions, with a faster and physiological repair of scar in test areas in relation to control area.
Keywords:
Burns. Wound Healing. Biotechnology. Hospitalization. Skin.
INTRODUÇAOA queimadura é uma lesao traumática que pode atingir o ser humano, além de ser uma das causas reiteradas de mortalidade, bem como de graves incapacidades a longo prazo. Constitui uma lesao dos tecidos orgânicos que pode resultar de traumas de origem térmica, química, elétrica e radioativa, desencadeando desde uma pequena bolha até formas graves. Pode levar à desfiguraçao, à incapacidade e, em muitos casos, até a morte
1.
A lesao provocada por queimaduras também pode ser descrita com base em sua profundidade, sendo classificada como de primeiro grau, quando compromete apenas a epiderme, apresentando eritema e dor, porém nao provoca alteraçoes hemodinâmicas; de segundo grau, quando atinge a epiderme e parte da derme, ocasionando a formaçao de flictenas, podendo ser de segundo grau superficial (atinge epiderme e, superficialmente, a derme, restando ainda os pelos, glândulas sudoríparas e sebáceas) ou de segundo grau profunda (acomete a porçao mais profunda da derme, restando geralmente apenas os pelos); ou ainda de terceiro grau, quando envolve todas as estruturas da pele, apresentando-se esbranquiçada ou negra, pouco dolorosa e seca
2.
O processo de cicatrizaçao ocorre para restaurar a integridade anatômica e funcional do tecido, de forma que o organismo lança mao de um complexo mecanismo que envolve quimiotaxia, divisao celular, neovascularizaçao, síntese de matriz proteica extra-celular e remodelaçao da cicatriz. Na dinâmica cicatricial, a síntese de colágeno inicia-se no terceiro dia, atinge seu pico em três a seis semanas e entra na fase de remodelaçao. Nesta fase, o colágeno tipo III é o primeiro a ser sintetizado e, à medida que ocorre maturaçao do tecido, é gradativamente substituído pelo colágeno tipo I. Nessa fase, ocorre formaçao do epitélio e contraçao da ferida em virtude da proliferaçao celular
3.
A cicatrizaçao ocorrerá toda vez que a perda de tecido for além da derme, iniciando-se com a fase inflamatória. Essa fase é a preparaçao da ferida para o reparo tecidual. Há uma agregaçao das plaquetas e depósito de fibrina, formando um coágulo sobre a lesao. A fibrina forma uma rede onde as células podem subir e infiltrar-se na área que está cicatrizando. Os neutrófilos, linfócitos e macrófagos migram sobre a rede de fibrina com o objetivo de remoçao de tecidos desvitalizados
1.
As membranas de colágeno sao absorvíveis e degradáveis, bem como possibilitam a nutriçao das células que preenchem o tecido afetado e o acesso das células de defesa ao local, permitindo adesao, migraçao e proliferaçao celular
4. Além disso, essas membranas funcionam como sistema de liberaçao controlada de fármacos, sendo concebidos para se obter uma adequada concentraçao plasmática ou níveis de concentraçao tecidual de fármacos de forma controlada, atingindo o efeito terapêutico desejado e evitando possíveis reaçoes tóxicas inerentes aos produtos
5,6.
A partir de estudo prévio
7 envolvendo a cicatrizaçao de queimaduras em humanos com a utilizaçao da membrana bioativa de colágeno contendo ácido úsnico incorporado em lipossomas, e sabendo-se que este produto mostrou-se eficaz, seguro e de qualidade, a atual pesquisa justifica-se pela necessidade de se conhecer e testar a aplicabilidade desta abordagem terapêutica na cicatrizaçao de queimaduras em áreas especiais, tais quais regiao palmar e plantar, bem como face, uma vez que existem no mercado poucos recursos disponíveis para a regeneraçao tecidual nessas áreas.
Em estudo anterior
8, observou-se que os filmes de colágeno e gelatina contendo ácido úsnico promoveram, de forma eficaz, a melhora da cicatrizaçao de queimaduras utilizando modelo animal. Além disso, sugere-se que esta melhora esteve relacionada à modulaçao de alguns eventos biológicos envolvidos neste processo, tais como a resposta inflamatória, a epitelizaçao e a formaçao de colágeno. Com isso, tornou-se relevante investigar o efeito deste biomaterial em modelo humano, a fim de constatar a eficácia do produto, bem como a sua segurança na utilizaçao em pacientes acometidos por queimadura, com efeitos positivos no processo de cicatrizaçao e qualidade de epitelizaçao, suscitando a necessidade de continuidade com estudos terapêuticos ampliados.
O objetivo geral deste estudo foi avaliar o efeito das membranas bioativas de colágeno contendo ácido úsnico incorporado em lipossomas no processo de cicatrizaçao de queimaduras em áreas especiais, descrever as características das queimaduras dos pacientes admitidos na Unidade de Tratamento de Queimados e comparar o efeito da membrana com o medicamento utilizado atualmente na prática clínica como produto de referência (curativo com sulfadiazina de prata ou óleo à base de ácido graxo essencial), por meio da mensuraçao da área da ferida.
MÉTODOTrata-se de um estudo de intervençao, descritivo e de campo, de comparaçao intraindividual, utilizando abordagem quantitativa com análise qualitativa de imagens como critério complementar de avaliaçao. A pesquisa foi realizada na Unidade de Tratamento de Queimados (UTQ) do Hospital de Urgência de Sergipe (HUSE), em Aracaju, SE. Este local foi escolhido por apresentar uma infraestrutura necessária para a execuçao da pesquisa, além de ser referência no atendimento destinado a pacientes vítimas de queimaduras no estado de Sergipe e áreas circunvizinhas. O setor possui uma ala masculina, composta por quatro leitos; outra ala feminina, com mais quatro leitos; uma ala infantil, com quatro leitos; um isolamento e um centro cirúrgico. Todas as alas sao climatizadas e equipadas com tubulaçao de oxigênio, vácuo e ar comprimido.
A amostra foi por conveniência, após análise prévia de prontuários para triagem, baseada nos critérios de inclusao e exclusao. Foi composta por nove pacientes (n=9), sendo 7 do sexo masculino e 2 do sexo feminino, com queimaduras de segundo grau profundo, que se encontravam hospitalizados na unidade de queimados. Os pacientes foram recrutados durante o período de três meses, sendo coletados dados gerais e clínicos dos mesmos e selecionados de acordo com critérios de inclusao e exclusao estabelecidos. Vale ressaltar que a randomizaçao das áreas foi feita com uso de tabela de números aleatórios, sendo a avaliaçao intraindividual e o paciente controle dele mesmo. As áreas variaram entre face, regiao palmar e plantar.
Assim, os indivíduos apresentavam duas áreas queimadas: área teste (membrana bioativa de colágeno contendo ácido úsnico incorporado em lipossomas) e área controle (sulfadiazina de prata, em regiao palmar e plantar, ou óleo à base de ácido graxo essencial, em face). Os critérios de inclusao foram pacientes em idade superior a 18 anos, sendo preconizada uma idade limite de 85 anos, de ambos os sexos, sendo observados fatores interferentes na cicatrizaçao das queimaduras, tais como: estado nutricional do paciente, presença de doenças subjacentes, como diabetes, alteraçoes cardiovasculares, coagulativas, aterosclerose, insuficiência renal e condiçoes infecciosas sistêmicas.
O projeto foi enviado ao Comitê de Ética em Pesquisa (CEP), através da Plataforma Brasil, tendo recebido aprovaçao sob parecer de número 459.541 e o CAAE de número 22896413.4.0000.5546, seguindo as normas da Resoluçao nº 466/2012 do Conselho Nacional de Saúde (CNS) do Ministério de Saúde sobre pesquisas envolvendo seres humanos, os preceitos éticos quanto à legitimidade das informaçoes, privacidade e sigilo das mesmas. Os pacientes e/ou responsáveis foram devidamente informados sobre a pesquisa de forma clara e objetiva e voluntariamente assinaram o Termo de Consentimento Livre e Esclarecido (TCLE), tendo a opçao de absterem-se da pesquisa em qualquer momento que desejassem.
Os pacientes do estudo foram recrutados e avaliados por anamnese e exame físico das áreas. Os dois grupos foram analisados quanto ao seu desfecho (cicatrizaçao de queimaduras), sendo essa observaçao feita inicialmente antes da primeira intervençao (T0 e C0) e reavaliados após 14 dias da abordagem (T14 e C14), visto que a maioria dos eventos que acompanharam o processo de cicatrizaçao está concentrada nesses períodos
9.
As membranas bioativas foram produzidas pelas próprias pesquisadoras no Laboratório de Ensaios Farmacêuticos e Toxicidade (LeFT) da Universidade Federal de Sergipe (UFS), seguindo método de preparaçao previamente descrito
8. Após confecçao em diâmetro de 7 cm e embaladas, foram submetidas a processo de esterilizaçao por radiaçao ionizante. Os pacientes foram avaliados macroscopicamente para estudo clínico do processo de reparo.
A captura das imagens foi feita de forma padronizada nos tempos 0 (T0 e C0) e 14 (T14 e C14), com máquina fotográfica digital da marca Cyber-shot 5.1 MP - SONY
®, posicionada a 40 cm da lesao, perpendicularmente à sua superfície. Foram eleitas as áreas mais evidentes de queimadura para o estudo. O paciente foi posicionado funcionalmente no leito para intervençao.
Nove pacientes participaram do estudo, sendo utilizada a membrana bioativa (área teste) e a sulfadiazina de prata ou óleo à base de ácido graxo essencial (área controle) para posterior análise qualitativa e descriçao macroscópica das lesoes em ambos os grupos após o início do tratamento, a fim de ser registrado sob a forma de painel.
Dentre os aspectos avaliados, estao o grau da queimadura, o agente causal, a localizaçao, o tipo de tecido presente no leito da ferida, a epitelizaçao das bordas, pigmentaçao, quantidade e característica do exsudato, a descriçao do procedimento terapêutico realizado e a periodicidade da troca de curativo, sendo essas variáveis verificadas através da avaliaçao clínica descritiva. Tanto na área teste quanto na área controle foi realizada a cobertura diariamente, uma vez ao dia, aplicada sempre pelo mesmo pesquisador, sendo necessária a utilizaçao de cobertura secundária.
Em seguida, procedeu-se à análise quantitativa com o uso de um programa de Imagem
(Image J
®). Esse programa consiste em um
software processador e analisador de imagens em Java de domínio público, inspirado no
NIH Image para o Apple Macintosh. Dessa forma, pode ser executado em diversos ambientes operacionais desde que os mesmos possuam uma máquina virtual Java apropriada. A investigaçao com o
Image J® tem o objetivo de quantificar a área lesada, bem como analisar as características do tecido. Esse programa de análise de imagem é de domínio público e pode ser utilizado para avaliaçao da contraçao das lesoes em tratamento.
Após a coleta, os dados foram tabulados em uma planilha do Microsoft Excel
® 2016. Para análises, foram utilizadas frequências e porcentagens, sendo os resultados apresentados sob a forma de tabelas, figuras e painéis. Os dados obtidos a partir da análise da determinaçao da intensidade da reaçao inflamatória e reepitelizaçao da superfície da área lesionada foram comparados entre os dois grupos nos tempos 0 e 14. Os valores médios obtidos a partir da análise quantitativa do diâmetro das feridas foram comparados entre os grupos, prefixando-se o nível de significância em 95% (p<0,05).
RESULTADOSA amostra foi composta por sete (77,8%) indivíduos do sexo masculino e dois (22,2%) do sexo feminino, sete (77,8%) da raça branca, com média de idade de 46,5 anos, sendo que seis (66,7%) das queimaduras ocorreram em ambiente intradomiciliar. Quanto à procedência, oito (88,9%) foram oriundos de municípios circunvizinhos, enquanto um (11,1%) foi proveniente de Aracaju. Dos nove (100%) pacientes estudados, um (11,1%) foi submetido à enxertia na área controle, nao sendo executado este procedimento nas áreas submetidas à aplicaçao da membrana. Quanto ao agente etiológico, as queimaduras foram causadas, em sua maioria, por líquidos inflamáveis (44,5%), seguido de choque elétrico (22,2%), chama direta (22,2%) e líquidos quentes (11,1 %).
Em relaçao à análise clínica descritiva das lesoes, ambos os grupos apresentaram, inicialmente (T0 e C0), uma superfície cruenta de bordas irregulares e mal definidas, recobertas por pseudomembrana fibrinosa. Em alguns casos, havia descontinuidade da pseudomembrana, deixando expostas áreas eritematosas ulceradas. Após início da abordagem terapêutica, nota-se maior presença de tecido de granulaçao na área teste, bem como maior vascularizaçao.
No 14° dia, observou-se epitelizaçao em ambas as áreas, entretanto, a regiao teste (T14) mostrou-se com cicatrizaçao mais homogênea e mais avançada, enquanto a área controle (C14) ainda se apresentava com mais exsudato e deposiçao de fibrina. Esse aspecto observado na área teste é provavelmente resultado do aumento da neovascularizaçao, irrigando a nova estrutura dérmica e estimulando o processo de cicatrizaçao das bordas para o centro da ferida.
Assim, foi possível observar melhor qualidade na cicatrizaçao da área teste (T14) nos pacientes analisados, com relevo plano e regular, ao contrário do grupo controle (C14), no qual as irregularidades de relevo foram mais evidentes, assim como áreas de eritema típicas de reaçao de granulaçao em evoluçao.
A Figura 1 evidencia o padrao progressivo de reduçao da área das queimaduras ao longo do tempo nos dois grupos analisados com o uso do programa
Image J®, com área visivelmente mais reduzida no grupo teste (de 2,769 cm
2 para 1,258 cm
2) em relaçao ao grupo controle (de 2,882 cm
2 para 2,091 cm
2).
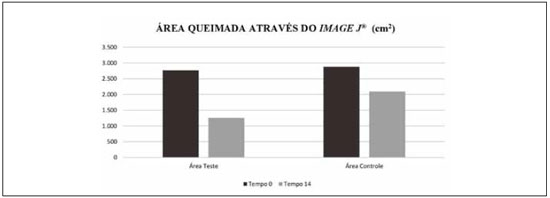 Figura 1
Figura 1 - Area da queimadura nos grupos teste e controle nos tempos 0 (T0 e C0) e 14 (T14 e C14).
Em pesquisa realizada anteriormente
7, o processo de cicatrizaçao ocorre para restaurar a integridade anatômica e funcional do tecido, de forma que o organismo lança mao de um complexo mecanismo que envolve fase inflamatória, divisao celular, neo-vascularizaçao, síntese de matriz proteica extracelular e remodelaçao da cicatriz. Dados do Ministério da Saúde apontam que, embora a sulfadiazina de prata continue sendo o padrao-ouro no tratamento de queimadura tópica, estudos recentes indicam que esta pode atrasar a cicatrizaçao de feridas, uma vez que é classificada como antimicrobiana e nao cicatrizante, sendo uma das únicas referências, dentre os medicamentos de uso tópico disponíveis pelo Sistema Unico de Saúde (SUS), para tratamento de queimaduras.
De acordo com Dai et al.
10, um problema associado à sulfadiazina de prata refere-se à resistência bacteriana, sendo relatadas espécies
Pseudomonas resistentes a essa substância. Nesta pesquisa, foi utilizada a membrana bioativa de colágeno contendo ácido úsnico incorporado em lipossomas como uma alternativa inovadora em se tratando de queimaduras em áreas especiais, uma vez que estudo recente
7 indicou que este produto natural representa uma alternativa eficaz no tratamento de queimaduras dérmicas em humanos, porém ainda nao havia sido aplicada em áreas especiais, como face, regiao palmar e plantar.
Dentro desse contexto, Ragonha et al.
11 acrescentam que o comprometimento das maos e dos pés pode evoluir com incapacidade funcional. Os curativos oclusivos caracterizam-se pela aplicaçao de uma cobertura primária seguida por outra secundária. Esse tipo de curativo tem como vantagem permitir a mobilizaçao do paciente. O método aberto é mais utilizado em pacientes críticos com mobilidade limitada e em locais de difícil oclusao, como face e orelha.
Apresenta como vantagem, dependendo do tipo de cobertura, a possibilidade de visualizaçao da área queimada, facilidade na mobilizaçao de articulaçoes, baixo custo e simplicidade na aplicaçao. Em relaçao às desvantagens, apresenta grande risco de levar o paciente à hipotermia, sobretudo em grandes queimados, requerendo maior temperatura externa, necessidade de diversas aplicaçoes diárias e dificuldade de manipulaçao do paciente.
Neste estudo, as vítimas de queimadura foram, em sua maioria, do sexo masculino, com predomínio de lesoes provocadas por agentes inflamáveis, seguido de choque elétrico e chamas de fogo e, em menor proporçao, por líquidos quentes, ocorridas no ambiente domiciliar, sendo a maior proporçao desses pacientes oriundos de áreas circunvizinhas. Esses achados corroboram as pesquisas realizadas por Nascimento et al.
12 e Echevarría-Guanilo et al.
13, as quais encontraram resultados semelhantes ao atual estudo.
Após a ocorrência da queimadura, o organismo responde com uma série de eventos fisiológicos, em uma tentativa de restabelecer a continuidade epitelial. Na presente pesquisa, observou-se uma cascata de eventos envolvidos no reparo tecidual, sendo descritos como cicatrizaçao mais homogênea e mais avançada, com menos exsudato e deposiçao de fibrina formando o tecido de granulaçao, resultando em aumento da neovascularizaçao, irrigando a nova estrutura dérmica e estimulando o processo de reepitelizaçao das bordas para o centro da ferida.
Alguns autores
8,14 apontam a importância de curativos oclusivos, como filmes de colágeno/gelatina utilizados como barreira mecânica na cicatrizaçao de feridas. Jayakumar et al.
15 descreveram que o produto para lesao na pele deve apresentar características biológicas adequadas, dentre elas, atuar como uma barreira protetora contra micro-organismos e agentes no meio externo.
Elsner et al.
16 ainda ressaltaram que um bom curativo deve agregar a capacidade oclusiva à biodegradabilidade, além de permitir a incorporaçao de fármacos bioativos. Estudos prévios
7,8 demonstraram que o recobrimento de feridas com filmes biocompatíveis acelera a formaçao da reaçao de granulaçao em modelos experimentais e humanos de cicatrizaçao dérmica. Esses resultados foram ratificados com o atual estudo, o qual utilizou a membrana bioativa de colágeno/gelatina em áreas especiais.
Contudo, para Lee & Robinson
5, a incorporaçao do ácido úsnico em lipossomas pode sugerir que a liberaçao mais lenta da membrana, em comparaçao à rápida liberaçao da prata veiculada sob forma de creme, pode prolongar a sua atividade biológica, favorecendo a cronificaçao da inflamaçao e o desenvolvimento da reaçao de granulaçao. Alguns autores
7,8 afirmam que filmes de colágeno e gelatina possibilitam a incorporaçao de compostos ativos com atividade antimicrobiana e/ou anti-inflamatória para liberaçao gradativa e, caso os mesmos sejam incorporados em lipossomas, podem atuar como sistemas de liberaçao controlada, concebidos para obtençao de adequada concentraçao plasmática ou níveis de concentraçao tecidual de fármacos de forma controlada, atingindo o efeito terapêutico desejado e evitando possíveis reaçoes tóxicas inerentes ao composto.
Em duas pesquisas
17,18, a avaliaçao visual foi comparada com a planimetria computadorizada para medir a porcentagem de fibrina, sendo as estimativas muito semelhantes. Tal resultado implica que a descriçao subjetiva do quadro clínico no que diz respeito à epitelizaçao pode ser mais bem utilizada para efeito, em detrimento da avaliaçao com a imagem digital, uma vez que esta é demorada e, portanto, sua utilidade clínica na prática diária é limitada. Em geral, ambos os métodos possuem desvantagens, no entanto, acreditamos que as deficiências encontradas na análise de imagens digitais enfatizam a importância da avaliaçao clínica subjetiva.
CONCLUSAOObservou-se, com a utilizaçao da membrana de colágeno contendo ácido úsnico incorporado em lipossomas, maior degradaçao de fibrina, com deposiçao de tecido de granulaçao, acelerando a cicatrizaçao das bordas para o centro da ferida. Alicerçado neste estudo e em pesquisas anteriores, evidenciou-se que a análise por imagem tem grande importância na descriçao mais precisa do processo de cicatrizaçao. Entretanto, a avaliaçao clínica, embora subjetiva, ainda continua sendo o recurso mais utilizado, pela sua praticidade e por ser de melhor avaliaçao, com achados muito semelhantes àqueles obtidos através da análise por imagem.
Sendo assim, este estudo constitui de relevância científica, uma vez que existem no mercado poucos recursos disponíveis para a cicatrizaçao tecidual, particularmente em áreas especiais, como face, regiao plantar e palmar, o que contribui para a necessidade de se conhecer e testar a aplicabilidade desta abordagem terapêutica. No entanto, devido à escassez de pesquisas clínicas voltadas à cicatrizaçao, sugerem-se novos estudos com uma amostra mais representativa.
REFERENCIAS1. Andrade AG, Lima CF, Albuquerque AKB. Efeitos do laser terapêutico no processo de cicatrizaçao das queimaduras: uma revisao bibliográfica. Rev Bras Queimaduras. 2010;9(1):21-30.
2. Evers LH, Bhavsar D, Mailänder P. The biology of burn injury. Exp Dermatol. 2010;19(9):777-83.
3. Gainza G, Villullas S, Pedraz JL, Hernandez RM, Igartua M. Advances in drug delivery systems (DDSs) to release growth factors for wound healing and skin regeneration. Nanomedicine. 2015;11(6):1551-73.
4. Parenteau-Bareil R, Gauvin R, Cliche S, Gariépy C, Germain L, Berthod F. Comparative study of bovine, porcine and avian collagens for the production of a tissue engineered dermis. Acta Biomater. 2011;7(10):3757-65.
5. Lee TWY, Robinson JR. Sistema de Liberaçao Controlada de Drogas. In: Gennaro AR, ed. Remington - a Ciência e a Prática da Farmácia. 20ª ed. Rio de Janeiro: Guanabara Koogan; 2014. p. 933-60.
6. Pires ALR, Bierhalz ACK, Moraes AM. Biomaterials: types, applications and market. Quím Nova. 2015;38(7):957-71.
7. Costa ACSM. Estudo clínico piloto do efeito de membranas de gelatina contendo ácido úsnico incorporado em lipossomas no processo de cicatrizaçao de queimaduras [Tese de doutorado]. Sao Cristóvao: Universidade Federal de Sergipe; 2017.
8. Nunes PS, Albuquerque RL Jr, Cavalcante DR, Dantas MD, Cardoso JC, Bezerra MS, et al. Collagen-based films containing liposome-loaded usnic acid as dressing for dermal burn healing. J Biomed Biotechnol. 2011;2011:761593.
9. Oosterwijk AM, Mouton LJ, Schouten H, Disseldorp LM, van der Schans CP, Nieuwenhuis MK. Prevalence of scar contractures after burn: A systematic review. Burns. 2017;43(1):41-9.
10. Dai T, Huang YY, Sharma SK, Hashmi JT, Kurup DB, Hamblin MR. Topical antimicrobials for burn wound infections. Recent Pat Antiinfect Drug Discov. 2010;5(2):124-51.
11. Ragonha ACO, Ferreira E, Andrade D, Rossi LA. Avaliaçao microbiológica de coberturas com sulfadiazina de prata a 1%, utilizadas em queimaduras. Rev Lat Am Enferm. 2005;13(4):514-21.
12. Nascimento LKA, Barreto JM, Costa ACSM. Unidade de Tratamento de Queimados: perfil epidemiológico dos pacientes admitidos na Fisioterapia. Rev Bras Queimaduras. 2013;12(3):177-81.
13. Echevarría-Guanilo ME, Goncalves N, Farina JA, Rossi LA. Avaliaçao da qualidade de vida relacionada à saúde no primeiro ano após a queimadura. Esc Anna Nery. 2016;20(1):155-66.
14. Banyard DA, Bourgeois JM, Widgerow AD, Evans GR. Regenerative biomaterials: a review. Plast Reconstr Surg. 2015;135(6):1740-8.
15. Jayakumar R, Prabaharan M, Sudheesh Kumar PT, Nair SV, Tamura H. Biomaterials based on chitin and chitosan in wound dressing applications. Biotechnol Adv. 2011;29(3):322-37.
16. Elsner JJ, Egozi D, Ullmann Y, Berdicevsky I, Shefy-Peleg A, Zilberman M. Novel biodegradable composite wound dressings with controlled release of antibiotics: results in a guinea pig burn model. Burns. 2011;37(5):896-904.
17. Gankande TU, Duke JM, Wood FM, Wallace HJ. Interpretation of the DermaLab Combo
® pigmentation and vascularity measurements in burn scar assessment: an exploratory analysis. Burns. 2015;41(6):1176-85.
18. Bloemen MC, Boekema BK, Vlig M, van Zuijlen PP, Middelkoop E. Digital image analysis versus clinical assessment of wound epithelialization: a validation study. Burns. 2012;38(4):501-5.
Recebido em
11 de Março de 2019.
Aceito em
17 de Junho de 2019.
Local de realização do trabalho: Universidade Tiradentes (UNIT), Aracaju, SE, Brasil.
Conflito de interesses: Os autores declaram não haver.